酒中氰化物的测定标准操作程序之静态顶空——气相色谱法(一)
静态顶空-气相色谱法
概述
氢氰酸(HCN),别名氯化氰,相对分子质量27.03。相对密度0.69。熔点一14℃
沸点26℃。闪点一17.8℃。蒸气密度0.94。蒸气压101.31kPa(760mmHg,25.8℃)蒸气与空气混合物爆炸限6%~41%。水溶液呈弱酸性。是一种具有苦杏仁特殊气味的无色液体。易溶于水、酒精和乙醚。易在空气中均匀弥散,在空气中可燃烧。氯化氢在空气中的含量达到5.6%~12.8%时,具有爆炸性。氯化氢为气体,其水溶液称氢氰酸。
氰化物拥有令人生畏的毒性,然而它们绝非化学家的创造,恰恰相反,它们广泛存在于自然界,尤其是生物界。氢氯酸和氯离子的毒性极大,进入人体后,能迅速地被血浆吸收和输送,具有很强的与铁、铜、硫以及某些化合物(在生理过程起重要作用)的关键成分结合的能力,从而对细胞色素氧化酶的活动产生抑制作用,使之不能吸收血液中的溶液氧,导致细胞窒息和死亡。
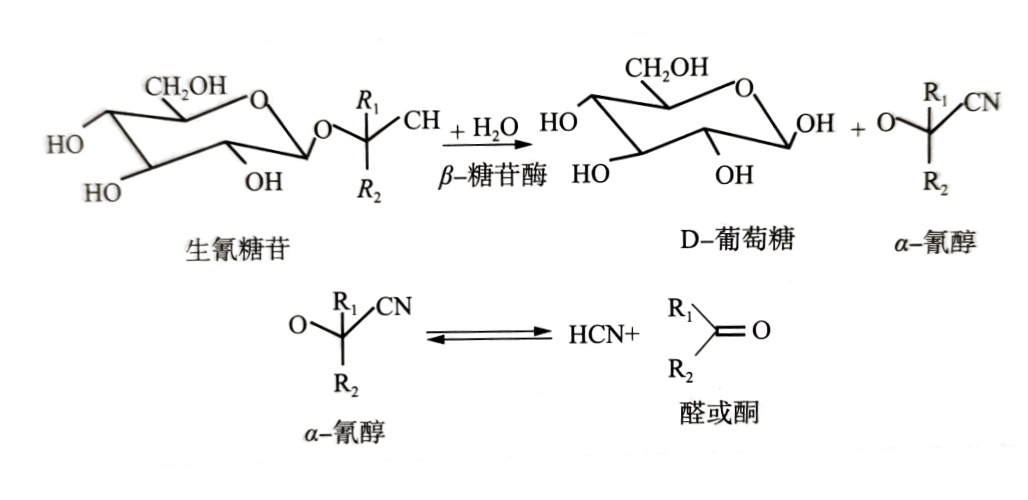
氯化物可由某些细菌,真菌或藻类制造,并存在于相当多的食物与植物中。在植物中,氯化物通常与糖分子结合,并以含氰糖甘( cyanogenic glycoside)形式存在。比如,木薯中就含有含氯糖苷,但当咀嚼或破碎含生氰糖苷的植物食品时,其细胞结构被破坏,使得一葡萄糖苷酶释放出来,水解生氯糖苷产生HCN,见图31,这便是食用新鲜植物引起氯氢酸中毒的原因,在食用前必须设法将其除去(通常靠持续沸煮)。水果的核中通常含有氯化物或含氯糖苷如杏仁中含有的苦杏仁苷,就是一种含氯糖苷,故食用杏仁前通常用温水浸泡以去毒。
酒中的氯化物大多由原料(如木薯、代用品、豆类及其他果核或混入一些野生植物)中含有的氯街类配糖体在发酵过程中水解产生。在不同pH的条件下,氯化物以分子氯(HCN)、氯离子(CN)及金属氯化物络合物形式存在。金属氯化物络合物又可分为弱络合金属氰化物和强络合金属氯化物(后者包括结构非常稳定的铁氯根离子和钴氯根离子)在碱性溶液中,自由氧化物将完全电离,成为氰离子:同时,形成稳定的金属络合氰化物。在中性或酸性溶液中,只有少部分自由氯化物发生离子化,多数以氢氰酸形式存在;当pH<4时,弱金属络合氰化物将分解为氢氰酸,而强金属络合氰化物则很难在室温下发生改变。因此,若要令强金属络合氰化物分解,需采取升温或增加酸含量的措施。
由于酒中的氰化物主要来自原料,而未成熟的作物籽粒,如未成熟的高粱籽粒及茎
叶内氯化物的含量就相对较高,尤其是以木薯、野生植物酿制的酒,氯化物含量较高。注重对酿酒原料的检測和监控,选用生氰糖苷含量较低的原料,从源头加以控制,可降低终产品中氢氯酸含量。
文章版权备注
- 2023-05-01奶味香精的制备技术与开发现状
- 2023-04-04阿魏酸及其衍生物在食品添加剂领域研究进展(一)
- 2023-03-23甘肃省榆中县市场监督管理局强化食品快检 筑牢食品安全防线
- 2023-03-23常德:专项整治酒类市场12种违法行为
- 2023-03-23贵州这7批次食品检出食品添加剂问题,有食用植物调和油、冰糖大蒜、无油剁椒等
- 2023-03-23怀化:部署开展制止餐饮浪费专项行动
- 2023-03-23超90%展商已确认展位 6月食品原料展带来海内外商机
- 2023-03-23关于召开2023年国际食品安全与健康大会的通知
- 2023-03-23河南省市场监管局召开落实食品安全“两个责任”暨制止餐饮浪费专项行动调度视频会议
- 2023-03-23邵阳市食品安全“两个责任”机制推进暨野生蘑菇中毒防控部署电视电话会议召开

 豫ICP备19024296号
豫ICP备19024296号 售前咨询
售前咨询