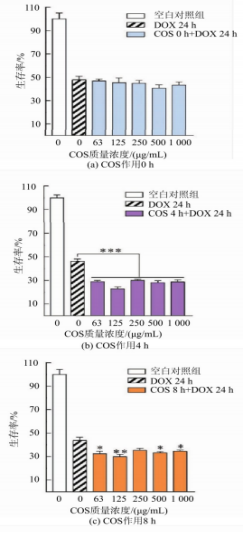
2.3.3 COS功效時间对其协同DOX抑止MDA-MB-231体细胞存活率的危害
在MDA-MB-231体细胞中,进一步剖析COS功效时问对体细胞存活率的危害。由图7所显示,与最初的状态下的体细胞存活率对比(见图7(a)),COS短期内功效后体细胞存活率明显减少,主要表现出提高体细胞对DOX敏感度的工作能力。在其中,给药時间4h标准下(见图7(b)),COS浓度值在0~125ug/mL时体细胞存活率呈浓度值依赖感降低,250~1000μg/mL时趋于平稳,与呈阳性药品DOX组对比均有很大的显著性差异(***P<O.001):功效8h(见图7(c)),COS浓度值在0~125μg/mL时体细胞存活率约降低20%,与DOX组对比有比较大显著性差异(**P<0.01),扩大浓度值在250~1000μg/mL时有显著性差异(*P<0.05)。再次增加时问至12h并无法减少体细胞的存活率(见图7(d))。COS在MDA-MB-231体细胞中提高其对阿霉素敏感度的体制尚需进一步剖析。
2.4 COS协同DOX抑止MDA-MB-231体细胞存活率的体制探析
2.4.1 COS对MDA-MB-231体细胞转移工作能力的危害
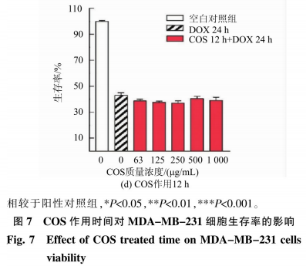
充分考虑MDA-MB-231体细胞的高转移特点,最先以小室转移试验身体之外调查COS能不能抑止肿瘤干细胞蔓延。如图所示8所显示,500μg/mLCOS功效后,相比于试剂空白组(NC),COS组的体细胞转移总数显著降低(**P<0.01)。表明COS可高效抑止MDA-MB-231体细胞转移,这与Nam等报导的科学研究状况一致。除此之外,COS抑止肿瘤干细胞转移的情况也存有于成化学纤维HTl080体细胞和MCF-10A甲状腺鳞状上皮细胞。从而确定了COS抑止肿瘤干细胞转移的功效。
2.4.2 COS对DOX入核的危害
DOX功效于肿瘤干细胞时,做为拓扑异构酶Ⅱ缓聚剂,进到细胞质影响DNA复制而充分发挥。依靠DOX内置鲜红色莹光的特性,根据激光共聚焦显微镜观察复合型COS给药时,MDA-MB-231体细胞对DOX的摄入实际效果,結果如图所示9所显示。伴随着DOX功效时間的增加,不管是不是给药COS,体细胞内DOX莹光抗压强度均呈時间依赖感提高。进一步与复合型给药对比,1h时,2组都观查到略微的DOX入核量,且差别不显著。而在3h时,COS与DOX复合型给药组较DOX独立给药组表明出更强的核内鲜红色莹光。5h时,2组的细胞质内鲜红色莹光均做到最強但元明显差别。从而表明,COS具备推动DOX迅速聚集于MDA-MB-231细胞质的功效。推断这一全过程很有可能与COS带正电相关,因为电子效应靶向治疗更改了恶性肿瘤细胞质表层负向电子流,进而影响到数据信号传输通道。除此之外,COS的这类提高DOX诱发细胞衰老的效果也在负荷DOX的含COS纳米复合材料中被看到和报导。
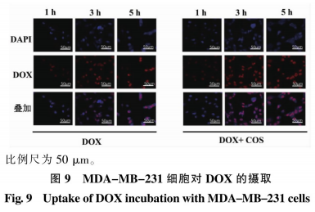
汇总之上結果能够推断,在MDA-MB-231体细胞中,COS与DOX的复合型给药根据控制肿瘤干细胞转移,并推动呈阳性药品DOX的入核而起到抗癌活力。二者的联用具备一定协作提质增效功效。
3 总结
COS具备优良的相容性和普遍的分子生物学活力。COS的抗癌功效是科研的网络热点,但其功效与体制因糖的构成及其细胞种类等而各不相同,必须进一步在特殊体细胞上讨论COS的功效与体制。
步在特殊体细胞上讨论COS的功效与体制。根据早期在细胞水平发觉的糖与化疗药联用提升疗效的分析結果,本科学研究中在酶法制取获得玻璃化温度2~4的低比较分子质量COS的根基上,选用COS与DOX复合型给药的方法点评COS的抗癌功效。身体之外抗癌活力点评数据显示,独立给药低浓度值COS对所选择的3株肿瘤干细胞并无明显抑止实际效果:当与DOX复合型给药时,低浓度值COS就可以明显减少人乳癌MDA-MB-231体细胞存活率。进一步的体制剖析推断了COS可根据抑止人乳癌体细胞转移,与此同时推动DOX入核而提高肿瘤干细胞对化疗药物的敏感度,充分发挥协作抗癌特点。这为作用糖等膳食补充剂与化疗药联用的治疗方案给予了数据信息参照和概念支撑点。
因为COS的抗癌功效与体制比较繁杂,受糖自身特性及其细胞株危害很大,将来针对COS抗癌功效的深层次分析也有待从特殊糖的构造、糖与体细胞功效的靶标、很有可能影响到的核心遗传基因和转录因子等分子结构水准进一步诠释和认证。
文章版权备注
- 2023-05-01奶味香精的制备技术与开发现状
- 2023-04-04阿魏酸及其衍生物在食品添加剂领域研究进展(一)
- 2023-03-23甘肃省榆中县市场监督管理局强化食品快检 筑牢食品安全防线
- 2023-03-23常德:专项整治酒类市场12种违法行为
- 2023-03-23贵州这7批次食品检出食品添加剂问题,有食用植物调和油、冰糖大蒜、无油剁椒等
- 2023-03-23怀化:部署开展制止餐饮浪费专项行动
- 2023-03-23超90%展商已确认展位 6月食品原料展带来海内外商机
- 2023-03-23关于召开2023年国际食品安全与健康大会的通知
- 2023-03-23河南省市场监管局召开落实食品安全“两个责任”暨制止餐饮浪费专项行动调度视频会议
- 2023-03-23邵阳市食品安全“两个责任”机制推进暨野生蘑菇中毒防控部署电视电话会议召开

 豫ICP备19024296号
豫ICP备19024296号 售前咨询
售前咨询