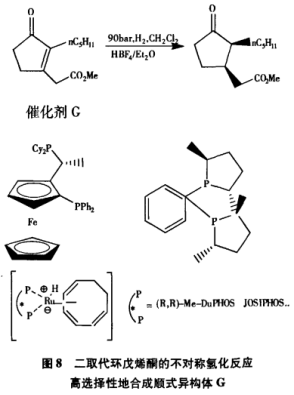
DobbsD—A等人采用特定的催化剂对脱氢茉莉酮酸甲酯进行不对称催化氢化(图8),他们采用的催化剂为手性膦化物,结果得到的顺式异构体与反式异构体之比都大于99/1,顺式异构体中c异构体的含量为82%。这种方法在提高c异构体的含量方面是一大进步,但是该方法要用到的催化剂制取有一定的难度,不适合大量生产。
3、以五元环类手性物质为起始原料合成顺式异构体
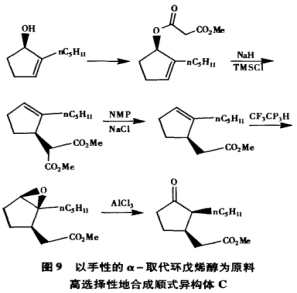
FirmenichSA等人用手性的环戊醇经过酯化重排脱羧,关键一步是用亲电的过氧酸氧化脱羧产物得到顺式的环氧,最后在路易斯酸作用下得到产品(图9)。这条路线的原料需要得到手性醇,这个醇可以由相应的酮用酶还原或用手性催化剂来还原。这条路线得到的C异构体的ee值高达98%,该途径的难点是手性醇的制备和顺式环氧化。
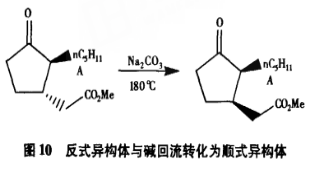
由于反式异构体与顺式异构体之间存在着热力学平衡,除了在pH为5~7这个范围内,式异构体通常比较容易转换为反式异构体,2000年KraftP等人采用反式二氢茉莉酮酸甲酯与碱(如碳酸钠)一起加热回流来提高顺式二氢茉莉酮酸甲酯的含量(顺式消旋体的含量达12.8%)(图10),进而提高C异构体的含量,该法很环保,很经济,但副反应严重影响香味稳定性且提高程度小。
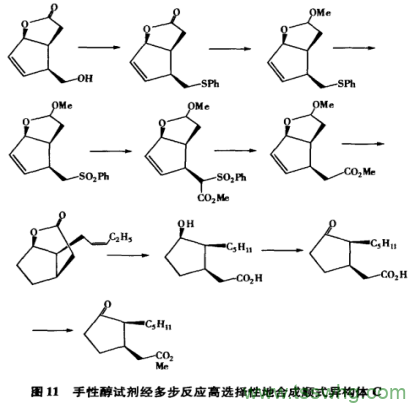
AlessioPorta等采用下列途径来合成C异构体,结果得到顺式/反式为99/1,顺式中C异构体的ee值高达93%(图11)。该途径存在的缺点是原料不易得到,路线长,总产率低。因此也不适合大量生产。
4、电化学的合成方法
Shono等介绍了一个复杂化合物在电解体系中闭环制取顺式一二氢茉莉酮酸甲酯与加氢原料取代环戊烯酮(图12)。但由于母体活性部位多,是目标产物的收率偏低。同时复杂母体的合成也比较困难,限制了该方法的推广价值。
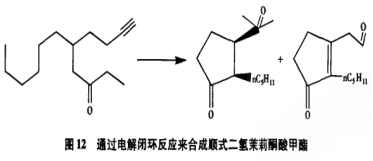
二、结语
以上我们讨论了以四种不同类型的化合物为原料制备顺式一二氢茉莉酮酸甲酯的方法,从中可以看出以环戊烯酮及其取代物为原料时,原料易得,且反应步骤少,只是需要高选择性的手性试剂作为催化剂。反观其它的合成路线,原料难得,反应条件苛刻,且产率也不高,所以KraftP等人提出了在合适的条件下反式异构体向顺式异构体的转化,该路线虽然目前产率还比较低,但它的合成路线具有潜在的实际应用价值,对该反应的动力学和热力学机理的研究推断,可以通过改变反应温度、pH值、溶剂等条件来提高顺式异构体的含量,如果推广到工业化。除了找到合成的最优条件外,实际生产中还需要设计出一套经济实用的工艺设备。
声明:本文所用图片、文字来源《中国食品添加剂》,版权归原作者所有。如涉及作品内容、版权等问题,请与本网联系
相关链接:脱氢茉莉酮酸甲酯,二氢茉莉酮酸甲酯,环戊烯
文章版权备注
- 2023-05-01不同贮藏方式对红香酥梨采后生理及品质的影响(一)
- 2023-05-01奶味香精的制备技术与开发现状
- 2023-05-01双孢蘑菇液体菌种发酵及栽培效果浅析
- 2023-05-01菌种强化结合工艺优化提高酱香白酒基酒中四甲基吡嗪含量的研究(二)
- 2023-05-01发酵小麦胚芽产2,6-二甲氧基对苯醌菌种筛选及发酵条件优化(一)
- 2023-05-01猕猴桃中铁含量的测定与测定因素的探究
- 2023-05-01腐植酸调节砷酸盐生菜毒性作用研究(四)
- 2023-05-01腐植酸调节砷酸盐生菜毒性作用研究(三)
- 2023-05-01腐植酸调节砷酸盐生菜毒性作用研究(二)
- 2023-05-01腐植酸调节砷酸盐生菜毒性作用研究(一)

 豫ICP备19024296号
豫ICP备19024296号 售前咨询
售前咨询