我们生活中常见的气体主要成分是甲烷,甲烷广泛分布于自然界,是天然气、甲烷、坑气及气体的主要成分之一。 它可以作为制造燃料及氢、一氧化碳、炭黑、乙炔、氰化氢及甲醛等物质。今天小编为大家讲解甲烷的化学性质与反应。
甲烷的化学性质与反应
1、氧化与燃烧
甲烷在常温时,不能被强氧化剂氧化,但在高温时能在空气中燃烧,发出淡蓝色火焰,同时分子破裂,碳原子和氢原子分别与空气中的氧结合,生成二氧化碳和水,并释放出大量的热:
CH4+2O2 → (燃烧)CO2+2H2O+热
甲烷燃烧时产生的热和光就是我们用作动力和照明的基础。但是,事物总是一分为二的,当甲烷与空气混合并在含甲烷5~14%时,遇火花就会发生猛烈的爆炸,煤矿瓦斯爆炸实际上就是甲烷可燃性所造成的不利的一面在起作用。但只要采取改善矿井通风条件,使矿井中甲烷含量不在上述比例范围内就可避免事故发生。
当甲烷在空气不足时燃烧,会产生大量黑烟,这叫做不完全燃烧,工业上利用这个原理,以甲烷为原料来制取炭黑:
CH4+O2 → (不完全燃烧)C+2H2O
炭黑大量用作增强橡胶耐磨性的填充剂,也是黑色颜料、油漆、油墨和墨汁的原料。
2、裂解反应
在没有空气存在的情况下,给甲烷施以高温,甲烷分子便会破裂“分家”,这种反应叫做裂解反应。例如,甲烷在1000~1200℃高温下生成炭黑和氢气。如果温度再高,两个甲烷分子又会转化成含两个碳原子的乙炔:
CH4 → (1000~1200℃)C+2H2
2CH4 → (1500℃)H-C≡C-H(乙炔)+3H2
乙炔是非常重要的有机化工原料。工业上利用天然气来生产乙炔是今后发展的方向。副产物氢气还可用做合成氨等的原料。
3、与水反应
甲烷和水蒸汽在高温与催化剂的存在下作用,生成一氧化碳和氢气:
CH4+H2O → (镍,860~900℃)CO+3H2
一氧化碳和氢气的混合气称为合成气。工业上利用天然气来制造氮肥,主要是将甲烷转化为合成气,再用其中的氢气与空气中的氮气化合成氨(NH3)。合成气也是制造甲醇(CH3OH)的重要原料。
4、卤代反应
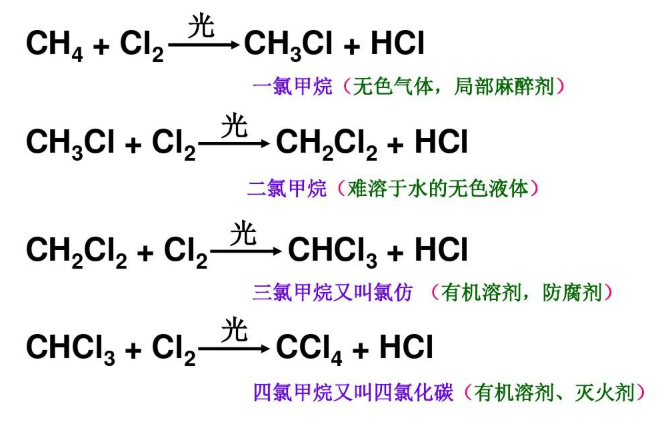
烃类分子中的氢原子被其他原子或原子团所取代的反应叫做取代反应。取代反应是有机化学中的基本反应之一。在取代反应中,烃类的氢原子如被卤素(Cl、Br等原子)所取代则叫做卤代反应。例如,甲烷与氯气在散射光的作用下(不能由日光直接照射)发生卤代反应,生成一氯甲烷、二氯甲烷、三氯甲烷与四氯化碳的混合物:
要使这些混合物彼此分离是比较困难的,但在工业生产上,可以用控制反应时的条件如调节氯气和甲烷的用量来使某一卤代产物成为主要产物。这些产物除都可用作有机溶剂外,其中三氯甲烷还是制造“塑料王”聚四氟乙烯的重要原料,而四氯化碳又可用作灭火剂。
以上内容便是小编为大家整理的甲烷的化学性质与反应知识了,希望能解答你对甲烷的疑问。
文章版权备注
- 2023-05-01不同贮藏方式对红香酥梨采后生理及品质的影响(一)
- 2023-05-01奶味香精的制备技术与开发现状
- 2023-05-01双孢蘑菇液体菌种发酵及栽培效果浅析
- 2023-05-01菌种强化结合工艺优化提高酱香白酒基酒中四甲基吡嗪含量的研究(二)
- 2023-05-01发酵小麦胚芽产2,6-二甲氧基对苯醌菌种筛选及发酵条件优化(一)
- 2023-05-01猕猴桃中铁含量的测定与测定因素的探究
- 2023-05-01腐植酸调节砷酸盐生菜毒性作用研究(四)
- 2023-05-01腐植酸调节砷酸盐生菜毒性作用研究(三)
- 2023-05-01腐植酸调节砷酸盐生菜毒性作用研究(二)
- 2023-05-01腐植酸调节砷酸盐生菜毒性作用研究(一)

 豫ICP备19024296号
豫ICP备19024296号 售前咨询
售前咨询