原甲酸三乙酯
- 所属分类: 资料库
- 产品标签: 原甲酸三乙酯使用标准 , 原甲酸三乙酯厂家 , 原甲酸三乙酯生产厂家
- 促销信息: 暂无
0
- 特别说明:产品图片以及参数跟实际产品略有差异
- 定制说明:一切规格按照客户实际情况或考察后量身定制,支持非标定制。
- 库存配送:有货,全国送货保障!
- 温馨提示:本产品一经下单生产,非质量问题不支持退货!
| 物竞编号 | 03F3 |
|---|---|
| 分子式 | C7H16O3 |
| 分子量 | 148 |
| 标签 |
三乙氧基甲烷;原甲酸乙酯, 脂肪族羧酸及其衍生物 |
CAS号:122-51-0
MDL号:MFCD00009230
EINECS号:204-550-4
RTECS号:RM6475000
BRN号:605384
PubChem号:24886840
1.性状:无色透明液体,有辛辣的气味。[9]
2.熔点(℃):-61[10]
3.沸点(℃):145.9[11]
4.相对密度(水=1):0.89[12]
5.相对蒸气密度(空气=1):5.11[13]
6.饱和蒸气压(kPa):1.33(40.5℃)[14]
7.辛醇/水分配系数:1.2[15]
8.闪点(℃):30(CC);35(OC)[16]
9.引燃温度(℃):180[17]
10.爆炸上限(%):25.1[18]
11.爆炸下限(%):0.7[19]
12.溶解性:微溶于水,溶于乙醇、乙醚等多数有机溶剂。[20]
13.常温折射率(n25):1.3900
14.气相标准燃烧热(焓)(kJ·mol-1):-4405.9
15.气相标准声称热(焓)( kJ·mol-1) :-635.3
16.液相标准燃烧热(焓)(kJ·mol-1):-4359.90
17.液相标准声称热(焓)( kJ·mol-1):-681.32
1.急性毒性[21] LD50:7060mg/kg(大鼠经口);20ml(17800mg)/kg(兔经皮)
2.刺激性[22]
家兔经皮:500mg(24h),轻度刺激。
家兔经眼:100mg(24h),中度刺激。
1.生态毒性 暂无资料
2.生物降解性 暂无资料
3.非生物降解性 暂无资料
1、摩尔折射率:39.67
2、摩尔体积(cm3/mol):163.5
3、等张比容(90.2K):367.0
4、表面张力(dyne/cm):25.3
5、介电常数:
6、偶极距(10-24cm3):
7、极化率:15.72
1.疏水参数计算参考值(XlogP):无
2.氢键供体数量:0
3.氢键受体数量:3
4.可旋转化学键数量:6
5.互变异构体数量:无
6.拓扑分子极性表面积27.7
7.重原子数量:10
8.表面电荷:0
9.复杂度:51.6
10.同位素原子数量:0
11.确定原子立构中心数量:0
12.不确定原子立构中心数量:0
13.确定化学键立构中心数量:0
14.不确定化学键立构中心数量:0
15.共价键单元数量:1
1.对水气很敏感,易燃,具有较强的挥发性和刺激性气味,应该在通风橱中使用。
2.稳定性[23] 稳定
3.禁配物[24] 强氧化剂、水、强酸
4.避免接触的条件[25] 潮湿空气
5.聚合危害[26] 不聚合
储存注意事项[27] 储存于阴凉、通风的库房。远离火种、热源。库温不宜超过37℃。保持容器密封。应与氧化剂、酸类等分开存放,切忌混储。采用防爆型照明、通风设施。禁止使用易产生火花的机械设备和工具。储区应备有泄漏应急处理设备和合适的收容材料。
1.乙醇钠法:以乙醇钠和氯仿为原料,在60-65℃下反应,生成原甲酸三乙酯粗制品,再经分馏精制得成品。
2.乙醇法:以乙醇和氢氧化钠代替乙醇钠,采用固-液相转移催化法,催化剂为PTC。
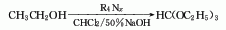
3.苯甲酰氯法:以苯甲酰氯、甲酰胺和无水乙醇为原料,在催化剂的作用下,生成原甲酸三乙酯、苯甲酸和氯化铵的混合物,经分离得到成品原甲酸三乙酯和苯甲酸。
4.在装有80厘米长的回流冷凝器的5升圆底烧瓶中放3升无水乙醇和490克(327毫升,4 .1摩尔)氯仿,烧瓶应放在易用流水冷却的位置。将207克(9克原子)洁净的金属钠切成小坟,使其可以适于从冷凝器中落下,然后在大约两小时内加入溶液中。为了要按这个速度加入金属钠,在加钠的时候必须使烧瓶冷却。当金属钠已完全作用,混合物也已冷至室温时,使用干燥仪器用吸滤法滤去氯化钠,用200毫升无水乙醇洗涤在滤纸上的氧化钠,使洗涤液流入上面得到的滤液中。
把滤液放在装有80厘米分馏柱的3升烧瓶中,在蒸汽浴或水浴上蒸出过量的氯仿和大部分的乙醇。将馏出物收集在2升吸滤瓶中,吸滤瓶上装有干燥箫,用以隔绝湿气。蒸馏需要5至6小时。在蒸馏巾收回的氯仿和乙醇的混合物重约2000克,可留在下次实验中使用。烧瓶中剩下的液体用倾析法除去少量氛化钠,倒入带有30厘米分镭柱的克氏烧瓶中,常压下蒸馏。85℃以下的馏分主要是乙醇,将共弃去;85-140℃的馏分约100克,其中约含有原甲酸乙醋总产一冠的四分之一。可以把这部分分馏,不过最好是合并在下一次实验的产物中。原甲敌醋在140-146℃之lbj蒸馏出来,重120~140克(27-31%)。
在第一次实验以后,在收回的氯仿一乙醇混合物中加入400克氯仿相足够的无水乙醉(800-1000毫升),使总体和达到3升。然后和前面一杆加入金属钠。在过量的氯仿和乙醇已从蒸馏柱中蒸馏出来以后,把上次实验的中间部分加进去,然后再进行分馏。这一次实验的产量约为200克45%。
1.原甲酸三乙酯是化学实验室常用的烷基化试剂和甲酰化试剂。它们易于储存,但反应活性很高。它们可以作烷基化试剂,很容易将烷基转移到各种醇羟基上;作甲酰化试剂时,在酸性或碱性条件下都可以使用。
与醇发生烷基化反应 原甲酸三乙酯作为烷基化试剂时,可以使各种醇发生相应的烷基化反应。可以使多元醇发生烷基化反应,生成相应的环状原甲酸酯 (式1)[1~3]。
醛或酮的保护 原甲酸酯可以用来保护醛和酮,生成甲酸酯和相应的缩醛或缩酮 (式2)[4,5]。
甲酰化反应 Lewis酸催化下,原甲酸酯可以作为甲酰化试剂, 与其它甲酰化试剂相比,具有操作简便,产率较高等特点。原甲酸酯在酸催化下,容易原位生成二烷氧基正碳离子,可以直接用于甲酰化反应。此类甲酰化反应可以在羰基邻位的α-C上 (式3)[6]。
与烯醇(或类似物)反应 烯醇的硅醚 (式4)[7] 或酮的烯醇盐 (式5)[8] 可以与原甲酸酯原位生成的正碳离子反应,生成β-缩醛基酮类化合物。
2.用于有机合成和用作医药中间体及感光材料。[28]
危险运输编码:UN 2524 3/PG 3
危险品标志: 刺激
刺激
安全标识:S16 S26
危险标识:R10 R36
1. Kazuhiko, T.; Kazuo, O.; Kazunori, T.; Kiyoshi, T.; Youichi, S. Chem. Pharm. Bull., 2000, 48, 1903.
2. Wu, W. D.; Bergstrom, D. E.; Davisson, V. J. J. Org. Chem., 2003, 68, 3860.
3. Gan, H.; Horner, M. G.; Hrnjez, B. J.; McCormack, T. A.; King, J. L.; Gasyna, Z.; Chen, G.; Gleiter, R.; Yang, N. C. J. Am. Chem. Soc., 2000, 122, 12098.
4. Waizumi, N.; Stankovic, A. R.; Rawal, V. H. J. Am. Chem. Soc., 2003, 125, 13022.
5. Manetsch, R.; Zheng, L.; Reymond, M. T.; Woggon, W.-D.; Reymond, J. L. Chem. Eur. J., 2004, 10, 2487.
6. David A. E.; Regan J. T. J. Am. Chem. Soc., 2005, 127, 10506.
7. Molander, G. A.; Jeffrey, S. C. Tetrahedron Lett., 2002, 43, 359.
8. Montalbetti, C.; Savignac, M.; Bonnefis, F.; Genet, J. P. Tetrahedron Lett., 1995, 36, 5891.
[1~8]参考书:现代有机合成试剂;胡跃飞 付华 编著;化学工业出版社;ISBN 7-5025-8542-7
[9~28]参考书:危险化学品安全技术全书.第一卷/张海峰主编.—2版.北京;化学工业出版社,2007.6 ISBN 978-7-122-00165-8
暂无